Contenido principal
Alfa 57
La nanotecnología es la máxima expresión de la tendencia a la miniaturización que ha caracterizado a la electrónica durante las últimas décadas. Un nanómetro es una milmillonésima de metro, apenas un poco por encima del tamaño de los átomos. Este número también aborda el funcionamiento de la Comisión Internacional de Protección Radiológica (ICRP), una institución científica independiente, reconocida internacionalmente como la fuente más fiable de información y opinión en el ámbito de la protección radiológica. Presentamos igualmente las actividades que el CSN realiza en investigación y desarrollo dentro de su ámbito de actuación, a través de su Plan de I+D+i y de su participación en proyectos nacionales e internacionales.
En los apartados técnicos, un artículo está dedicado al proceso de migración de las Especificaciones Técnicas de Funcionamiento Mejoradas (ETFM) en las centrales nucleares españolas, que culmina en junio de este año. El segundo se centra en las lecciones aprendidas por parte del Consejo durante el desarrollo del Plan de Inversión en Equipos de Alta Tecnología Sanitaria (INVEAT).
Linfocitos armados contra el cáncer
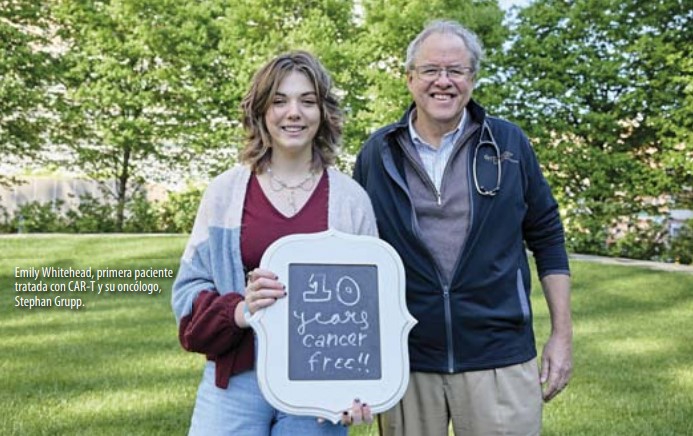
En los últimos años se ha desarrollado una técnica para el tratamiento de ciertos cánceres que concentra terapia celular, inmunoterapia y terapia génica en un mismo proceso y supone un avance importante en este campo. Se denomina terapia CAR-T y se aplica actualmente frente a cánceres hematológicos. En concreto, está aprobada contra la leucemia linfoblástica aguda, el linfoma de células B y el mieloma múltiple. Es la única alternativa para aquellos pacientes que han recaído tras recibir quimioterapia e, incluso, trasplante de médula ósea. Los investigadores estudian ahora otras posibilidades, como utilizar estas terapias en primera línea de tratamiento, identificar nuevas dianas contra éstos y otros tipos de cáncer e incluso utilizarlo contra tumores sólidos. Varios proyectos que se están llevando a cabo en diferentes unidades de investigación de nuestro país intentan avanzar en esos objetivos.
Texto: Noemí Trabanco | periodista de ciencia
E mily Whitehead fue la paciente número uno en el primer ensayo de terapia de células T con receptores quiméricos de antígenos (CAR-T, por sus siglas en inglés) contra la leucemia infantil. Tenía solo 6 años y tras una recaída sus posibilidades de supervivencia eran escasas. Casi 12 años después, Emily sigue libre de cáncer y la terapia CAR-T se ha convertido en un nuevo paradigma en el tratamiento del cáncer. El oncólogo Stephan Grupp, que lideró el ensayo en el Hospital de Niños de Filadelfia, en aquel momento en fase I, colaboraba estrechamente con el investigador Carl June, padre de esta tecnología. La Sociedad Americana de Oncología Clínica (ASCO) calificó la CAR-T como el Avance del Año en 2018.
Esta terapia se basa en la reprogramación genética de los linfocitos T del propio paciente, un tipo de glóbulo blanco cuya función es precisamente eliminar células infectadas y activar otros tipos celulares en la respuesta del organismo contra infecciones y otras enfermedades. A los linfocitos extraídos del paciente se les inserta un gen para que sean capaces de expresar una proteína en su membrana que funciona como receptor de otra proteína (antígeno) existente en las células cancerosas. Una vez reconocido este antígeno, los linfocitos son capaces de eliminarlas. Hasta el momento CAR-T se utiliza en el tratamiento del cáncer hematológico, que se produce en los tejidos a partir de los que se forma la sangre o en sus células inmunitarias.
La primera enfermedad para la que se demostró su eficacia fue la leucemia linfoblástica aguda (LLA) de tipo B, como la que presentaba Emily, donde la producción excesiva de linfocitos B inmaduros no permite la producción de leucocitos normales. Este tipo de leucemia es más común en niños y es el tipo de cáncer que más muertes provoca en menores de 15 años. “En España puede haber unos 300 casos al año, de los cuales no más de 30 o 40 necesitan acceder al CAR-T”, explica el doctor Antonio Pérez, jefe del servicio de Hemato-Oncología pediátrica del Hospital Universitario La Paz de Madrid, que también lidera el Grupo de Investigación Traslacional en Cáncer Infantil, Trasplante Hematopoyético y Terapia Celular del Instituto de Investigación Sanitaria (IdiPAZ) del mismo hospital.
En el caso de la leucemia, y también del linfoma de tipo B, el antígeno contra el que se dirigen los linfocitos es el denominado CD19. Actualmente existen varios CAR-T producidos por la industria farmacéutica y aprobados en diferentes partes del mundo contra tres tipos de cáncer: LLA de tipo B, linfoma de tipo B en adultos y el mieloma múltiple (cáncer que se inicia en las células plasmáticas en la médula ósea). “La tecnología CART ha evolucionado muy rápido a nivel de indicaciones médicas, pero en el caso de España, lo hace más lento a nivel de regulación, aunque en los últimos años el Ministerio ha comenzado a trabajar con más celeridad y se acaban de aprobar recientemente dos nuevas indicaciones”, indica el doctor Pérez. 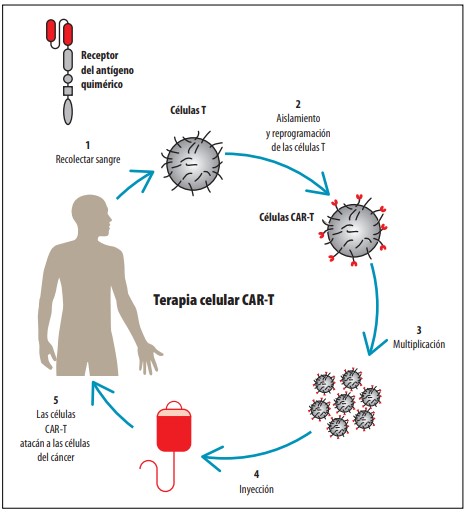
Este retraso ha supuesto que para algunos pacientes, especialmente adultos, fuese difícil acceder a este tipo de terapias. Actualmente la aplicación del tratamiento a través del Sistema Nacional de Salud (SNS) requiere de la aprobación de un comité evaluador y existen aún ciertas trabas burocráticas entre ésta y la aplicación del tratamiento. España cuenta hoy en día con más de 25 hospitales repartidos por todo el territorio, en los que se aplica esta terapia en adultos. Para cáncer infantil hay diez centros designados por el Ministerio. “A lo largo de estos años habremos tratado unos 500 pacientes para LLA, fundamentalmente niños”, detalla Antonio Pérez, que también es el coordinador del Grupo de Terapias Avanzadas del Grupo Español de Trasplante Hematopoyético y Terapia Celular (GETH).
Hasta el pasado año, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) había aprobado únicamente los CAR-T Kymriah y Yescarta, de las compañías farmacéuticas Novartis y Gilead, respectivamente. El pasado año se aprobaron también Tecartus (Gilead) y Abecma (Bristol Myers Squibb), este último contra mieloma múltiple, que muchos pacientes estaban esperando.
Hasta el momento, la terapia CAR-T se reserva para pacientes muy específicos, en los que se ha producido una recaída en una fase avanzada de la enfermedad. “Son pacientes que ya han recibido no una sino varias rondas de quimioterapia y algunos hasta dos y tres trasplantes de médula”, explica el doctor Pérez. En muchos de estos casos se trata de un tratamiento definitivo. Según los datos disponibles hasta el momento, transcurridos dos años tras su aplicación, un 48-50 % de los pacientes con LLA tratados siguen libres de enfermedad. “Algunos pacientes que fueron tratados en los primeros ensayos siguen libres de cáncer tras diez años y mantienen la memoria inmunológica, como ocurre en el caso de Emily Whitehead.
Desgraciadamente no siempre es así y, en algunos casos, los CAR desaparecen al cabo de unos meses. Esto obliga a dar otro tratamiento para consolidar esa respuesta, como puede ser un trasplante”, explica la doctora Susana Rives, jefa de la Unidad de Leucemias y Linfomas y de la Unidad CAR-T del Servicio de Hematología y Oncología Pediátrica del Hospital Sant Joan Déu, en Barcelona, donde han tratado a más de cien pacientes con esta terapia desde que llegara a España, entre ensayos clínicos y casos por indicación médica. En el linfoma este porcentaje es menor. “Aquí, no es tan importante que se mantenga esa memoria inmunológica, sino que las células T sean capaces de destruir al inicio, pero también existen casos en los que el tratamiento fracasa, alrededor de la mitad de los pacientes, bien porque no responden ya desde el inicio o bien porque recaen posteriormente. En estos casos aún no tenemos claro qué hacer después, pero ya es una mejoría con respecto a la quimioterapia o el trasplante, que no conseguía curar prácticamente a ningún paciente, y así podemos alargar el tiempo libre de enfermedad y mejorar la calidad de vida de algunos de ellos”, añade Rives.
Para evaluar su eficacia en la curación “hay que tener en cuenta que esta terapia se inició en 2012, y a España no llegó hasta 2016. Necesitamos más tiempo de seguimiento de los pacientes para poder evaluar su capacidad de curación. En leucemia linfoblástica existe riesgo de recaída incluso tras 5 o 10 años. Necesitamos un poco más de recorrido”, manifiesta Antonio Pérez, que añade “aun así, no debemos olvidar que ha blamos de pacientes para los que no había otra alternativa”.
La investigación, indispensable
Las terapias CAR-T pueden ser el único recurso para aquellos pacientes en los que otros tratamientos no han funcionado, incluidos los actualmente disponibles. Son, afortunadamente, muy pocos casos, pero esto hace difícil que la industria farmacéutica ponga interés en ellos. La investigación académica es indispensable para desarrollar nuevos CAR que den respuesta a estos casos. Un ejemplo es la leucemia linfoblástica de tipo T. En este caso “los pacientes tienen bastantes más dificultades que en el caso de la B. Es una enfermedad aguda y muy agresiva. La mayoría de los casos se cura con quimioterapia y/o trasplante, pero existe un cierto grupo de pacientes en los que esto no es suficiente. Nosotros estamos trabajando para desarrollar un CAR-T contra esta enfermedad”, explica Susana Rives.
Los denominados CAR-T académicos, desarrollados por grupos de investigación en hospitales y centros de investigación, requieren no obstante de una importante financiación, difícil de conseguir en muchos casos. Tanto la investigación preclínica como la realización de ensayos clínicos supone un coste muy elevado. “La financiación para la investigación académica viene fundamentalmente de las instituciones públicas, como la Agencia Estatal de Investigación o el Instituto de Salud Carlos III, pero también es fundamental el apoyo de fundaciones privadas. Un ejemplo fue el proyecto ARI, que dio a luz al CAR-T ARI-0001, desarrollado por el Hospital Clínic de Barcelona, o los proyectos que hemos llevado a cabo o que desarrollamos actualmente con la Fundación CRIS Contra el Cáncer”, explica Antonio Pérez.
De esta fundación es director científico y patrón el médico e investigador Joaquín Martínez, jefe de Hematología del Hospital 12 de Octubre y jefe de la Unidad de Investigación Clínica de Tumores Hematológicos H12O-CNIO. “La fundación tiene ya casi 13 años de existencia. Su único objetivo es favorecer la investigación en cáncer y entre las acciones que promueve están las becas de excelencia para investigadores, ya sean clínicos o básicos”, explica. Dentro de las convocatorias anuales, alrededor de un 30 % de los proyectos son para terapias avanzadas. Y también está financiando de forma sostenida unidades de investigación, como la del Hospital La Paz, dirigida por Antonio Pérez, o la nuestra, en el Hospital 12 de Octubre”, añade. La fundación, está también presente en Inglaterra y Francia. En España ha financiado ya más de 20 millones de euros en investigación en cáncer durante estos años.
Desde que las terapias CAR-T comenzaron a aplicarse la investigación académica ha permitido a los especialistas aprender cómo seleccionar a aquellos pacientes para los que esta terapia puede ser más efectiva, así como a manejar los posibles efectos adversos que conlleva. “Durante la primera semana se genera lo que denominamos tormenta de citoquinas. Hemos aprendido a manejarla y, a día de hoy, la mortalidad relacionada con el tratamiento es muy baja, por debajo del 1-2 %”, explica Antonio Pérez. Durante este tiempo “ha habido un gran desarrollo académico”, añade el investigador, que actualmente busca mejorar las alternativas existentes y buscar otras aplicaciones.
Nuevas estrategias
Entre los objetivos de los investigadores están encontrar nuevos CD19 que presenten ventajas terapéuticas con respecto a los ya existentes o evaluar la prescripción en fases previas de la enfermedad, así como identificar nuevas dianas contra las que enviar a los linfocitos, incluso para otros tipos de cáncer. “En nuestro hospital estamos involucrados, entre otros, en un ensayo a nivel internacional para evaluar el uso de Kymriah en primera línea de tratamiento en niños para los que sabemos que por sus características tienen mucho riesgo de recaer y de necesitar un trasplante de médula”, explica Rives. El grupo de Antonio Pérez trabaja también en la utilización de CAR frente a tumores sólidos, en su caso el sarcoma, un tumor en el que se ha avanzado muy poco hasta ahora. “Aquí tenemos un CAR-T multidiana, que nos acaba de autorizar la AEMPS para realizar un ensayo clínico y para su producción. También estamos trabajando en distintos tipos de leucemias que denominamos huérfanas, por su baja incidencia y lo poco que se conoce sobre su tratamiento, o en las que, en lugar de células, los CAR sean partículas más pequeñas que tengan más facilidad para penetrar en tumores sólidos, menos efectos adversos y mayor efecto en la diana”, indica.
El grupo liderado por Luis Álvarez-Vallina, jefe de la Unidad de Investigación Clínica en Inmunoterapia del Cáncer del CNIO y el Hospital 12 de Octubre, ha desarrollado durante estos años una alternativa a los CAR-T tradicionales: las células STAb-T. Se trata de combinar los CAR-T junto a lo que se conoce como anticuerpos biespecíficos, que son capaces de reconocer dos dianas diferentes. De esta forma reconocen tanto las células cancerosas como otras células T. En este tipo de inmunoterapia contra el cáncer, los anticuerpos se administran directamente al paciente. “Obteniendo células T con anticuerpos biespecíficos aumentamos la capacidad de penetración en los tumores, que en el caso del tratamiento con anticuerpos es más baja, y podemos reclutar más linfocitos T en la proximidad, cosa que no ocurre con las células CAR-T”, explica el investigador. “A nivel preclínico, tanto in vitro como en modelos animales, hemos visto que esta estrategia potencia de forma muy importante la respuesta citotóxica”, añade. Hasta el momento lo han demostrado para leucemias y linfomas tipo B y también para mieloma múltiple. “Pensamos que esta estrategia puede ser complementaria a la estrategia CAR-T”, expone Álvarez-Vallina. 
Su colega, el doctor Joaquín Martínez, con el que colabora en algunos proyectos, trabaja en otra alternativa a las células T. En su grupo tratan de utilizar otro tipo de células inmunes, los linfocitos NK (del inglés natural killer), que hasta el momento resultaban más difíciles de manipular en laboratorio, pero que podrían resultar más eficaces y menos tóxicos en el proceso. Otra de sus líneas de investigación es la de evaluar el impacto de la microbiota en este tipo de tratamientos. “Parece que actúan como moduladores del sistema inmune. Así, ciertos tipos de microorganismos o los compuestos que éstos producen pueden potenciar el efecto de estas terapias mientras que otros pueden perjudicarlo”, explica Martínez. “Otra de las líneas de investigación en las que trabajamos es la de aplicar lo que denominamos CAR-T alogénicos, es decir, de donantes. Esto reduciría el tiempo del proceso y, además, no tenemos que obtener linfocitos de pacientes que se encuentran en un estado clínico susceptible”. Estas y otras posibles aplicaciones apuntan a un papel fundamental de la terapia CAR-T en el tratamiento del cáncer, e incluso otras enfermedades.

 Descarga la revista completa
Descarga la revista completa